Mayo Clinic: nuevo modelo de roedor para gen de ELA y demencia frontotemporal conlleva esperanza para posibles terapias
JACKSONVILLE, Florida: Los científicos de Mayo Clinic en Florida desarrollaron un modelo de roedor que muestra las características neuropatológicas y conductuales vinculadas con el tipo genético más común de la esclerosis lateral amiotrófica (ELA o enfermedad de Lou Gehrig) y de la demencia frontotemporal (FTD, por sus siglas en inglés), ocasionadas por una mutación en el gen C9ORF72.
Los científicos dicen que los resultados, informados hoy en Science, acelerarán la realización de investigaciones más profundas sobre el mecanismo molecular detrás de estos trastornos, y que el modelo de roedor ofrecerá un medio para analizar posibles sustancias terapéuticas que detengan la muerte de las neuronas en el cerebro y en la médula espinal.
“Nuestro modelo de roedor muestra las patologías y los síntomas de la ELA y de la demencia frontotemporal observados en los pacientes con la mutación C9ORF72”, comenta el autor principal del estudio, Dr. Leonard Petrucelli, quien ostenta el título de Profesor Ralph B. y Ruth K. Abrams y es director del Departamento de Neurociencias en Mayo Clinic de Florida.
Según la asociación de la ELA, más de 30 000 estadounidenses viven con esta enfermedad que destruye las neuronas motoras encargadas de controlar actividades musculares básicas como hablar, andar y tragar. La demencia frontotemporal, después de la enfermedad de Alzheimer, es el tipo más común de demencia de aparición temprana y se caracteriza por cambios en la personalidad, comportamiento y lenguaje debido a la pérdida de neuronas en el lóbulo frontal del cerebro. A pesar de que la demencia frontotemporal alguna vez fue considerada rara, ahora la Asociación de la Enfermedad de Alzheimer piensa que está presente en 10 a 15 por ciento de todos los casos de demencia.
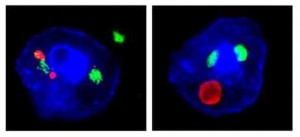
El nuevo modelo de roedor demuestra que la expansión repetida de C9ORF72, anomalía genética descubierta en 2011 por la investigadora de Mayo Dra. Rosa Rademakers, conduce a la producción de especies tóxicas de ácido ribonucleico (ARN) que forman focos anómalos o grupos, así como inclusiones de las proteínas c9RAN y TDP-43. El laboratorio Petrucelli descubrió la existencia de las proteínas c9RAN en los casos de demencia frontotemporal y ELA con mutación C9ORF72 (c9FTD/ELA) en el año 2013. Sin embargo, el nuevo estudio esclarece la vinculación entre la expansión repetida de C9ORF72 y las inclusiones de TDP-43, proteína conocida desde hace mucho por desviarse de su camino en la mayoría de casos de ELA y demencia frontotemporal. Además, se ha encontrado inclusiones de TDP-43 en los enfermos de Alzheimer y en quienes presentan lesiones en la cabeza o sufren repetidas conmociones cerebrales.
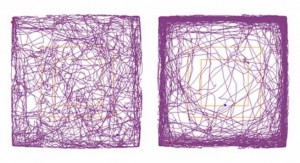
Los investigadores informan que estos cambios físicos y bioquímicos en el cerebro del roedor pueden ser los responsables de las deficiencias conductuales observadas y de los impedimentos motores afines a los síntomas de la enfermedad en los humanos. A los seis meses de edad, los ratones expresaron una expansión repetida de C9ORF72 en todo el sistema nervioso central, mostrando hiperactividad, ansiedad, comportamiento antisocial y deficiencias motoras.
“El descubrimiento de la TDP-43 en estos roedores fue completamente inesperado y sin este modelo de roedor, no se habría descubierto una vinculación entre la expansión repetida en C9ORF72 y el desarrollo de la patología TDP-43”, anota el Dr. Petrucelli.
“Esta observación es muy halagadora”, añade. “A pesar de que aún no sepamos cómo se vinculan los focos y las proteínas c9RAN a las anomalías de la TDP-43 ni cuál sea el camino que emplean, nuestro nuevo animal modelo ofrece ahora una manera de descubrirlo”.
A través de la colaboración con el Instituto de Investigación Scripps de Florida, el laboratorio Petrucelli también trabaja en la identificación de los componentes químicos que se unen al ARN de expansión repetida antes de formar los focos y las proteínas c9RAN que alteran la función neuronal. Al dirigir las terapias contra el ARN para prevenir la formación de focos de ARN y proteínas c9RAN en las células cerebrales, los colaboradores esperan combatir tanto la muerte celular como los síntomas de la enfermedad que sufren los pacientes con c9FTD/ELA. El modelo de roedor no solamente servirá para analizar novedosos componentes químicos, sino que los resultados del estudio en ratones plantean que un fármaco capaz de aliviar la toxicidad vinculada con los focos y las proteínas c9RAN también puede prevenir la patología de la TDP-43.
El trabajo se financió gracias al Instituto Nacional sobre el Envejecimiento [P50AG016574] de los Institutos Nacionales de Salud, al Instituto Nacional de Trastornos Neurológicos y Accidente Cerebrovascular [R21NS089979, R21NS084528, R21NS079807, R01NS063964, P01NS084974] de los Institutos Nacionales de Salud, a la Escuela de Estudios de Posgrado de Mayo, a la Asociación de ELA, al Centro Robert Packard para Investigación sobre la ELA en Johns Hopkins, al Target ALS y a la Asociación para la Enfermedad de Alzheimer.
Otros autores del trabajo son la primera autora Jeannie Chew, la Dra. Tania F. Gendron, la Dra. Mercedes Prudencio, el Dr. Hiroki Sasaguri, el Dr. Yong-Jie Zhang, Monica Castanedes-Casey, el Dr. Chris W. Lee, Karen Jansen-West, Aishe Kurti, la Dra. Melissa E. Murray, Kevin F. Bieniek, el Dr. Peter O. Bauer, Ena C. Whitelaw, Linda Rousseau, la Dra. Jeannette N. Stankowski, Caroline Stetler, Lillian D. Daughrity, Emilie A. Perkerson, la Dra. Rademakers; el Dr. Dennis W. Dickson, el Dr. John D. Fryer, Pamela Desaro, Amelia Johnstonn Karen Overstreet y el Dr. Kevin B. Boylan de Mayo Clinic en Florida. Participó también Dieter Edbauer,ç del Centro Alemán para Enfermedades Neurodegenerativas en Munich.
Los doctores Petrucelli y Gendron presentaron la documentación para solicitar la patente (No. 14/162,570) en Estados Unidos para el uso de poli(GP) inmunoensayos como diagnóstico para las enfermedades por expansión repetida del C9ORF72.
###
Información sobre Mayo Clinic
Mayo Clinic es una organización sin fines de lucro, dedicada a la investigación y educación médicas, que ofrece atención experta e integral a todos los que necesitan recobrar la salud. Si desea más información, visite https://www.mayoclinic.org/es/ y https://newsnetwork.mayoclinic.org/.
CONTACTO PARA LOS MEDIOS DE COMUNICACIÓN:
Soledad Andrade, Relaciones Públicas de Mayo Clinic, 507-284-5005, correo electrónico: newsbureau@mayo.edu
[mayoNnVideoDownload]







