


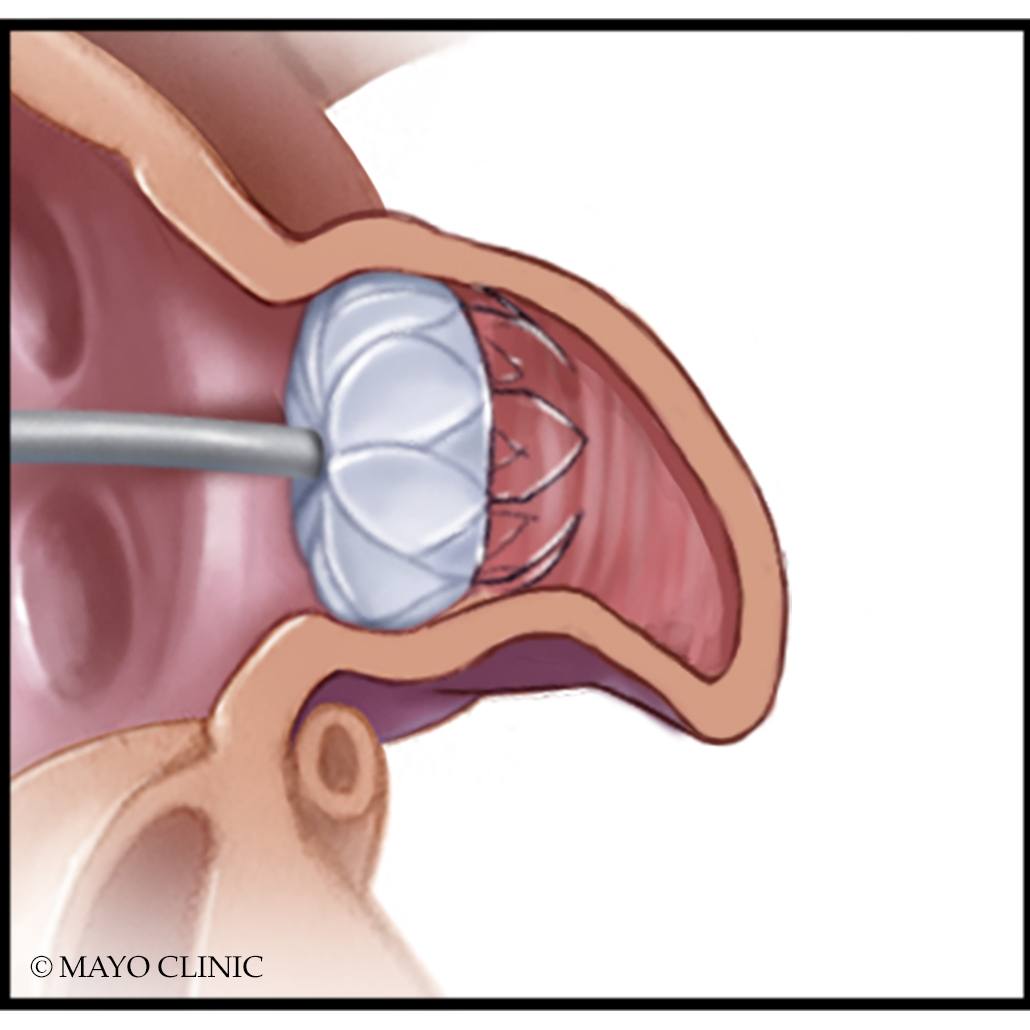
罗切斯特,明尼苏达州—妙佑医疗国际(Mayo Clinic)的一项新研究发现,左心耳封堵术渗漏的影响远比人们过去预想的更严重。这项研究发现,哪怕是极小的渗漏,也可能导致不良事件的发生风险增加10%–15%。美国心脏病学院发布的一篇新闻稿进一步概述了这项研究,并且研究结果已发表在《JACC:Clinical Electrophysiology》上。 左心耳是心脏左侧的一个不规则囊状结构,其中可能形成血栓。血栓若发生迁移,则可能会阻塞大脑中的动脉并阻断血流,从而导致中风。 人们通常使用抗凝剂来降低房颤患者中风的风险。但有些患者不适合长期接受这种疗法。个中原因包括药物相互作用、出血等副作用,或者必要临床检查相关的后勤工作。封堵左心耳开口能够大大降低患者中风的风险以及对抗凝剂的依赖,在房颤患者中尤其如此。 医生会小心植入Watchman装置来封堵左心耳开口,同时尽量避免出现可能降低其有效性的渗漏现象。妙佑医疗国际的介入性心脏病专家兼本研究的主要作者Mohamad Alkhouli医学博士表示,由于每个人的左心耳大小和形状都是独一无二的,这种手术后通常都会多少存在些许渗漏。 Alkhouli博士和研究人员指出,虽然仅有少数患者会在随访期间出现凝血相关问题,但我们必须继续改进以消除渗漏,并通过这种预防性手术进一步降低中风风险。 ACC的新闻稿进一步详细介绍了该研究的结果,并说明了成像和植入领域的医学进步能够如何改善这种手术的结局。 ### 致新闻工作者:Alkhouli博士可以接受英语和阿拉伯语采访。关于妙佑医疗国际全球服务信息可从此处获取。 关于妙佑医疗国际(Mayo Clinic)妙佑医疗国际是一所致力于创新并集临床实践、医学教育和科学研究为一体的非营利机构,以恻隐之心竭诚提供精湛医术和解决方案给需要治疗的每个人。请访问妙佑医疗国际新闻网,获取更多妙佑医疗国际的新闻信息。 媒体联系:请联系妙佑医疗国际公共事务部:Terri Malloy。邮箱:newsbureau@mayo.edu
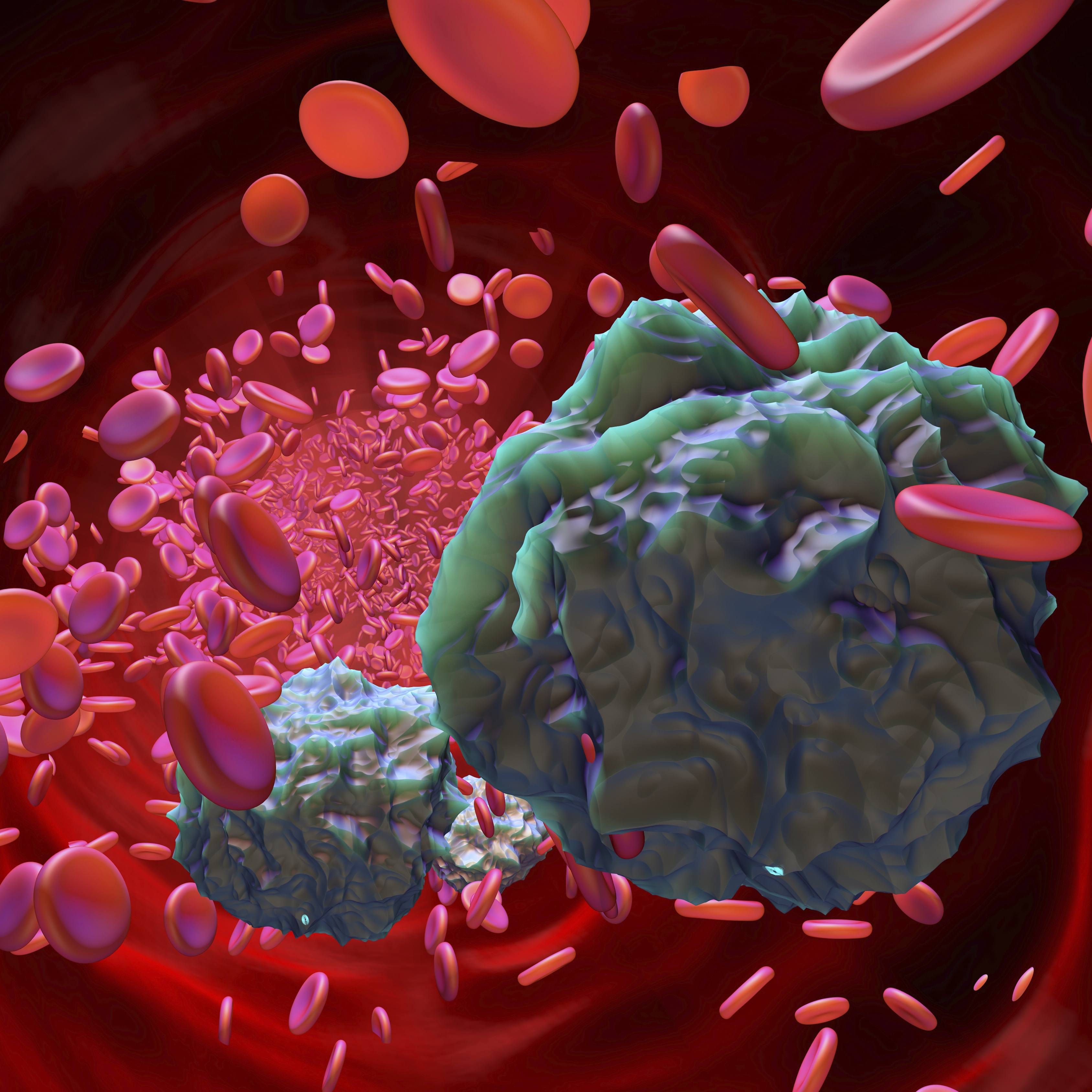
明尼苏达州罗切斯特 — 妙佑医疗国际(Mayo Clinic) 个体化医学中心(Center for individualized Medicine )的新研究发现,携带ASXL1突变体的慢性粒单核细胞白血病(一种罕见骨髓癌)患者中存在独特的表观遗传变化,可激活有害基因并导致癌细胞更快生长。ASXL1基因突变还能使疾病转化为更具侵袭性的急性髓细胞性白血病。 这项已在《自然-通讯》(Nature Communications)上发表的研究有助于阐明潜在的治疗策略并增进对ASXL1基因表达的了解。 表观遗传学是指细胞遗传物质的化学修饰过程,它控制着基因的表达方式并影响DNA编码的解读。研究已表明,表观遗传学在包括癌症在内的许多疾病的发展和进展中发挥关键作用。 “携带这些ASXL1基因突变的患者的表观基因组发生了变化,使癌细胞能够开启对患者有害的基因的表达。”妙佑医疗国际血液学家和科学家兼该研究的主要作者Moritz Binder医学博士表示。Binder医生是2021年Gerstner家庭职业发展(Gerstner Family Career Development)获奖者。 “这些表观遗传变化并不会影响DNA本身的蓝图,”Binder医生解释道。“但它会影响蓝图被阅读的方式,即哪些页需要阅读、哪些页不需要。” 慢性粒单核细胞白血病是一种通常影响60岁及以上人群的癌症。它源于骨髓的造血细胞并侵入血液。近40%的慢性粒单核细胞白血病患者伴有ASXL1基因突变。 “不幸的是,携带ASXL1突变的患者通常病况不佳,且对现有治疗的反应不如人意,”Binder医生道。 在这项研究中,Binder医生及其团队利用多种高通量测序技术进行了全面的多组学解析。多组学解析有助于了解构成疾病基础的信息流。 研究人员比较了携带和不携带ASXL1突变的患者的样本,并分析了其基因的活性以及DNA周围分子的特性。该研究还包括基因表达和影响DNA包装的多种修饰。 “这样我们就能进行建模,以此推断出表观遗传学变化在孤立和协同作用下对慢性粒单核细胞白血病ASXL1突变体中致白血病基因表达的影响。”Binder医生道。 总之,研究人员发现ASXL1突变与驱动白血病的关键基因的过表达有关。 Binder医生表示:“我们的研究支持一种观点,即几种重要的致白血病驱动基因处于基因组中调节元件的控制之下。”[...]
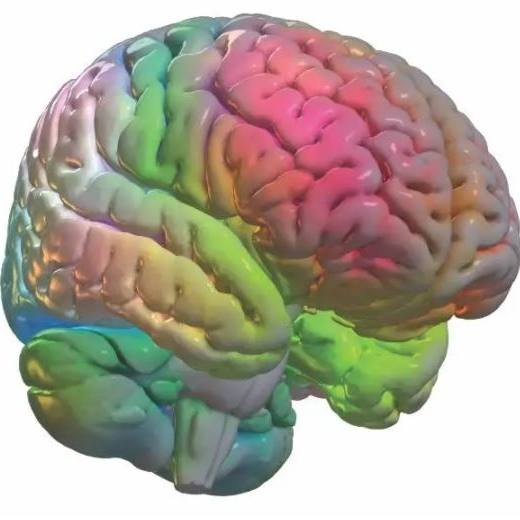
罗切斯特,明尼苏达州 — 妙佑医疗国际(Mayo Clinic) 研究人员提出了一种新的计算模型,用于在阿尔茨海默病症状与脑解剖结构之间建立起映射关系。该模型是通过将机器学习技术应用于患者大脑成像数据而开发的。这个模型利用大脑的完整功能,而不是特定的大脑区域或网络来解释脑解剖结构与心理过程之间的关系。研究结果已发表在《自然通讯》杂志上。 “这种新模型有助于我们进一步理解大脑在衰老和阿尔茨海默病期间的工作及受损原理,从而为监测、预防和治疗精神障碍提供新的方法,”妙佑医疗国际神经科医生及本研究的主要作者David T. Jones医学博士说。 阿尔茨海默病通常被描述为一种蛋白质加工问题。有毒蛋白质淀粉样蛋白和tau沉积在大脑区域,导致神经元衰竭,从而引发记忆丧失、沟通困难和思维混乱等临床症状。 然而临床症状、脑损伤模式和脑解剖结构之间的关系尚不明确。有些患者可能患有多种神经退行性疾病,这进一步加大了诊断的难度。使用该计算模型映射大脑行为可能会给临床医生提供新的视角。 为了开发这个新的模型,研究人员对妙佑医疗国际衰老研究和妙佑医疗国际阿尔茨海默病研究中心的423名认知受损的受试者进行了氟脱氧葡萄糖正电子发射计算机断层扫描(FDG-PET)脑葡萄糖测量。FDG-PET是一种显示葡萄糖如何为各大脑部位提供能量的成像检测技术。例如,阿尔茨海默病、路易体痴呆症和额颞叶痴呆症等神经退行性疾病都有着不同的葡萄糖利用模式。 该模型将与痴呆症症状相关的复杂脑解剖结构浓缩成一个概念性的颜色编码框架,以显示与神经退行性疾病和精神功能相关的大脑区域。这个模型中显示的成像模式与患者出现的症状有关。 目前已在410名患者中验证了该模型预测阿尔茨海默病生理变化的能力。另外,还通过映射正常衰老和痴呆综合征患者的大量数据,针对记忆、执行功能、语言、行为、运动、感知、语义知识和视觉空间能力进行了额外的验证。 研究人员发现,只需10种模式就能解释痴呆症患者大脑中51%的葡萄糖利用模式差异。这10种脑葡萄糖模式以独特组合出现在每个患者身上,具体取决于他们的症状类型。作为该研究的后续工作,Jones博士指导的神经学人工智能(AI)项目正在利用这10种模式来研究AI系统,以便帮助解读潜在阿尔茨海默病和相关综合征患者的脑部扫描评估影像。 “这种新的计算模型在经过深入验证并得到更多支持后,或许能够指引科学工作的方向,例如,指引大脑和痴呆症研究专注于复杂系统生物学的动力学,而不是错误折叠的蛋白质,”Jones博士说。 “如果与阿尔茨海默病相关的心理功能是在整个大脑中以分布式的方式执行,那么我们就需要一种像这样的新疾病模型。我们认为这种模型可能会推动人们对于神经退行性变与心理功能的诊断、治疗和基本理解。” 本研究的共同作者全部来自妙佑医疗国际,他们是:Val Lowe医学博士;Jonathan Graff-Radford医学博士;Hugo Botha医学士、外科学士;Leland Barnard博士;Daniela Wiepert;Matthew Murphy博士;Melissa Murray博士;Matthew Senjem;Jeffrey[...]